Los científicos podrían haber descubierto cómo se propaga la enfermedad de Parkinson a través del cerebro
Una nueva investigación sugiere que la propagación de la α-sinucleína tóxica en la enfermedad de Parkinson podría depender de mecanismos de transporte clave dentro de las neuronas. Los hallazgos apuntan a una posible estrategia para ralentizar la progresión de la enfermedad. Crédito: Shutterstock
Freda Kreier, Facultad de Medicina de Yale
Scitechdaily.com/
Investigadores han identificado dos proteínas en la superficie de las neuronas que podrían contribuir a la propagación de la enfermedad de Parkinson en el cerebro.
Una nueva investigación de la Facultad de Medicina de Yale (YSM) sugiere que dos proteínas presentes en la superficie de las neuronas cerebrales implicadas en el movimiento podrían desempeñar un papel clave en la progresión de la enfermedad de Parkinson.
La enfermedad de Parkinson es un trastorno neurodegenerativo en el que las neuronas se deterioran y mueren gradualmente. Esta pérdida celular está relacionada con la acumulación de α-sinucleína, una proteína que se pliega incorrectamente y puede propagarse de una neurona a otra.
Los científicos aún no comprenden del todo cómo se desplaza la α-sinucleína entre las células. Un nuevo estudio publicado en Nature Communications señala a dos proteínas de membrana, mGluR4 y NPDC1, como factores importantes que ayudan a transportar la α-sinucleína mal plegada a las neuronas sanas después de que sea liberada por las neuronas moribundas.
Stephen Strittmatter, MD, PhD. Profesor Vincent Coates de Neurología y Profesor de Neurociencia. Crédito: Facultad de Medicina de Yale.
El autor principal, Stephen Strittmatter, MD, PhD, profesor Vincent Coates de Neurología y director del Departamento de Neurociencia de la Facultad de Medicina de Yale, afirma que el descubrimiento podría contribuir al desarrollo de mejores tratamientos para el Parkinson.
La α-sinucleína mal plegada es «el rasgo patológico distintivo de la enfermedad de Parkinson», afirma. «Si entendiéramos cómo llega a las neuronas, quizás podríamos bloquear o ralentizar la progresión de la enfermedad», añade. Pero para ello, «necesitamos comprender el mecanismo molecular de su propagación».
Transporte de α-sinucleína
Las enfermedades neurodegenerativas, como el Alzheimer y el Parkinson, se están convirtiendo en un problema de salud cada vez mayor en Estados Unidos. La Fundación Parkinson estima que alrededor de 1,1 millones de personas en EE. UU. viven actualmente con la enfermedad de Parkinson, con casi 90 000 nuevos diagnósticos cada año.
La enfermedad de Parkinson suele causar síntomas relacionados con el movimiento, como temblores, problemas de equilibrio y lentitud en los movimientos. Estos síntomas están vinculados a la acumulación de α-sinucleína mal plegada en las células cerebrales motoras. A medida que la proteína se propaga de neurona en neurona, los síntomas empeoran.
Una posible vía por la que la α-sinucleína ingresa a nuevas células es mediante la unión a proteínas en la superficie celular. Para comprobar esta posibilidad, Strittmatter y sus colegas generaron 4400 grupos de células, cada uno diseñado para expresar diferentes proteínas de superficie, y examinaron si alguno de ellos se unía a la α-sinucleína mal plegada.
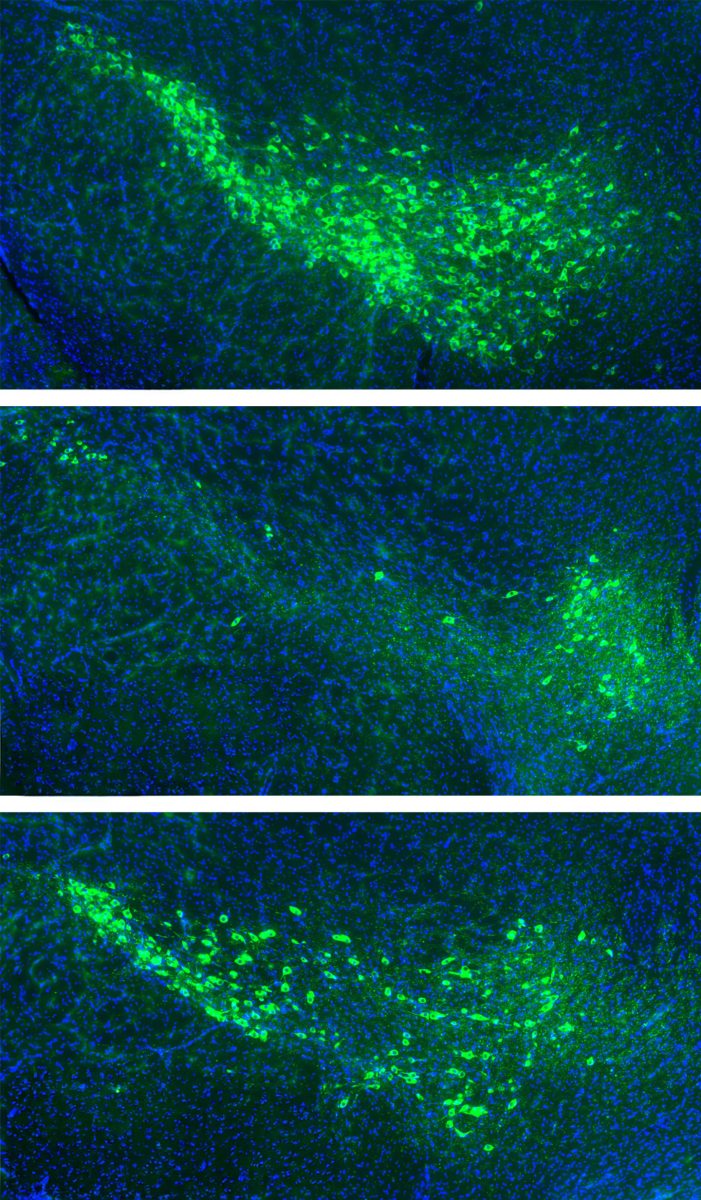
Arriba: Células dopaminérgicas (verdes) en la sustancia negra de ratones sanos. Centro: Las células dopaminérgicas degeneran en ratones expuestos a α-sinucleína mal plegada. Abajo: En ratones deficientes en mGluR4 y NPDC1, las células dopaminérgicas se conservan tras la exposición a α-sinucleína mal plegada. Crédito: Facultad de Medicina de Yale.
La mayoría de las proteínas de superficie no se unieron a ella. Sin embargo, 16 sí lo hicieron, incluidas dos que se encuentran en las neuronas dopaminérgicas humanas de la sustancia negra, la región cerebral que se degenera en la enfermedad de Parkinson. Los investigadores descubrieron que estas dos proteínas, mGluR4 y NPDC1, transportaban α-sinucleína mal plegada al interior de las células.
Prevención de la propagación de la patología del Parkinson
Los resultados llevaron a Strittmatter y sus colegas a sospechar que mGluR4 y NPDC1 podrían facilitar el desplazamiento de la α-sinucleína entre neuronas. Para investigar más a fondo, los investigadores modificaron genéticamente ratones para que mGluR4 o NPDC1 dejaran de funcionar, y luego les introdujeron α-sinucleína mal plegada.
En ratones normales, la α-sinucleína mal plegada introducida se acumuló en el cerebro y los animales desarrollaron síntomas similares a los del Parkinson. Los ratones que carecían de los receptores mGluR4 o NPDC1 funcionales no mostraron el mismo patrón. Los investigadores también descubrieron que la eliminación de los genes de estas dos proteínas de superficie en un modelo de ratón de la enfermedad de Parkinson redujo el riesgo de muerte y ralentizó la progresión de los síntomas.
En conjunto, los experimentos sugieren que mGluR4 y NPDC1 actúan conjuntamente para ayudar a transportar la α-sinucleína mal plegada a las neuronas de los ratones.
Strittmatter afirma que los hallazgos apuntan a una posible nueva vía para el tratamiento de la enfermedad de Parkinson. Las terapias actuales ayudan principalmente a controlar los síntomas, pero no detienen eficazmente la progresión de la enfermedad. Según él, atacar directamente la propagación de la α-sinucleína podría conducir a tratamientos que ralenticen o incluso detengan la enfermedad de Parkinson.
Estos tratamientos podrían adquirir mayor importancia en los próximos años. La enfermedad de Parkinson y otras afecciones neurodegenerativas afectan principalmente a los adultos mayores. A medida que aumente el número de estadounidenses mayores de 65 años en las próximas décadas, más personas tendrán un mayor riesgo de desarrollar la enfermedad de Parkinson.
“Tenemos una población que envejece. Detener o ralentizar la muerte neuronal es un problema enorme”, afirma Strittmatter. “Este es el momento de avanzar en la búsqueda de la manera de frenar este proceso”.
10 de mayo de 2026
_____________
Este trabajo fue financiado por la subvención 16257 de la Fundación Michael J. Fox a APC, y por las subvenciones R01AG034924, R35NS097283, R01AG070926, R01AG066165 y P30AG066508 de los NIH a SMS.
_____________
Referencia:
“El complejo mGluR4-NPDC1 media la neurodegeneración inducida por fibrillas de α-sinucleína” por Azucena Perez-Canamas, Mingming Chen, Leire Almandoz-Gil, Nabab Khan, Si Jie Tang, Allyson Ho, Erik C. Gunther y Stephen M. Strittmatter, 25 de diciembre de 2025, Nature Communications .
___________
Fuente: