Alzheimer temprano: un fármaco lo bloquea 60 días antes de que aparezcan los síntomas
El NU-9 detiene la inflamación cerebral en ratones en etapas tempranas de la enfermedad de Alzheimer. Actúa décadas antes de la pérdida de memoria.
Gianluca Riccio
futuroprossimo.it /Diciembre 22 2025
Una pastilla cada mañana, durante dos meses. Luego, la inflamación desapareció, las proteínas tóxicas se disolvieron y la memoria permaneció intacta, al menos en pruebas con ratones. NU-9, la pequeña molécula inventada en la Universidad Northwestern, no espera a la aparición temprana del Alzheimer. Lo previene. Funciona cuando el cerebro todavía está sano, cuando nadie se acuerda de olvidar, cuando las placas amiloides recién han aparecido.
El estudio, publicado esta semana en Alzheimer y demencia, identifica un subtipo de proteína particularmente agresivo: ACU193+Esta variante se forma dentro de las neuronas estresadas, migra a los astrocitos cercanos y desencadena una cascada inflamatoria. La proteína NU-9 es capaz de interceptarla antes de que cause daño: es una profilaxis, no una cura. Funciona si tomas el medicamento cuando aún no sabes que estás enfermo.
Alzheimer temprano: el problema comienza décadas antes
La neurodegeneración no es un acontecimiento repentino. Daniel Kranz, primer autor del estudio de Northwestern, lo dice claramente:
“El Alzheimer temprano comienza décadas antes de que aparezcan los síntomas, con oligómeros de beta-amiloide1 tóxicos que se acumulan en las neuronas y células gliales que se vuelven reactivas mucho antes de la pérdida de memoria”.
Cuando aparece el primer olvido, las pruebas cognitivas que señalan un problema, el daño ya está avanzado. Esta es la razón por la que muchos ensayos clínicos fracasan: intervienen demasiado tarde.
La idea detrás de NU-9 es diferente. Tratar el Alzheimer de inicio temprano antes de que se convierta en una enfermedad grave significa interceptar la enfermedad en un período en el que el cerebro aún funciona, pero las proteínas tóxicas ya han comenzado a acumularse. En la práctica, se necesita un biomarcador que indique el riesgo y un medicamento para tomar inmediatamente después.
En el modelo de ratón presintomático utilizado por los investigadores, NU-9 redujo significativamente la gliosis astrocítica reactiva, una reacción inflamatoria que comienza mucho antes de los síntomas de la enfermedad de Alzheimer temprana.
Los oligómeros de beta-amiloide unidos a los astrocitos se desplomaron. Y la forma anormal de la proteína TDP-43, asociada con el deterioro cognitivo, también disminuyó drásticamente.
ACU193+, la proteína que lo desencadena todo
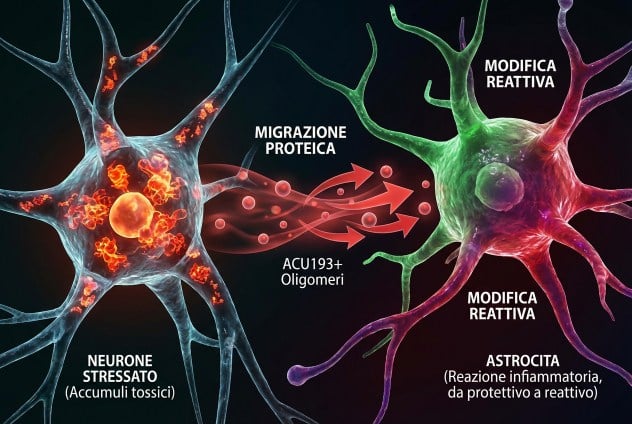
Los oligómeros ACU193+ se desprenden de las neuronas estresadas y convierten a los astrocitos en enemigos. NU-9 los detiene antes de que den el salto.
No todos los oligómeros de beta-amiloide son iguales. Durante décadas, los investigadores consideraron que estos agregados proteicos eran más tóxicos que las placas fibrosas que se forman posteriormente. Pero el equipo de Northwestern descubrió algo nuevo: Existe un subtipo particularmente agresivo, detectable mediante el anticuerpo ACU193. Aparece tempranamente, dentro de las neuronas estresadas. Luego migra a los astrocitos, las células con forma de estrella que se supone protegen a las neuronas. Y una vez allí, se desata el infierno.
Los astrocitos, normalmente aliados del cerebro, se vuelven hostiles al activarse. Liberan moléculas inflamatorias, dañan las sinapsis y aceleran la neurodegeneración. Detener este proceso es una de las formas más poderosas de retardar la progresión del Alzheimer en sus primeras etapas. E NU-9 hace exactamente eso: Reduce los oligómeros ACU193+ e impide la activación de los astrocitos. En esencia, desactiva la mecha antes de que explote.
Del laboratorio a la clínica: ¿qué falta?
ricardo silverman, el inventor de NU-9 (y anteriormente de Lyrica, un fármaco para la fibromialgia y el dolor neuropático), trabajó en esta molécula durante 15 años. en 2021NU-9 ha demostrado eficacia contra la ELA al eliminar las proteínas tóxicas SOD1 y TDP-43. en 2024La FDA de EE. UU. autorizó ensayos clínicos para la ELA. A principios de este año, el equipo demostró que el NU-9 también es eficaz contra la enfermedad de Alzheimer temprana en cultivos de células hipocampales. Ahora se realiza este estudio en ratones presintomáticos.
¿El siguiente paso? Probar si funciona en humanos. Y lo más importante, comprender si existe una forma fiable de identificar a las personas en riesgo antes de que presenten síntomas. «Si alguien tiene un biomarcador que indica Alzheimer en etapa temprana, podría empezar a tomar NU-9 antes de que aparezcan los síntomas», explica Silverman.
Es el mismo enfoque que se adopta con el colesterol: no se espera a que ocurra un ataque cardíaco, se reduce el colesterol mientras todavía se está bien.
Hoja de estudio
- Organización de investigación: Universidad del Noroeste
- Investigadores principales: Daniel Kranz, William Klein, Richard Silverman
- Año: 2025
- Rivista Alzheimer y demencia: The Journal of the Alzheimer's Association
- Enlace: Comunicado de prensa de Northwestern
- TRL: 4 – Se completaron con éxito los ensayos preclínicos en modelos animales
El mecanismo: salvar las células antes de que mueran
¿Cómo funciona el NU-9 a nivel celular? Las células cuentan con un sistema para eliminar las proteínas dañadas. En enfermedades neurodegenerativas como la ELA y el Alzheimer de inicio temprano, este sistema falla. Las proteínas tóxicas se acumulan, forman agregados y dañan las estructuras celulares. El NU-9 restaura esta vía. No elimina los síntomas; protege la célula desde dentro. Por eso funciona tanto para la ELA como para el Alzheimer de inicio temprano: ambas enfermedades comparten el mismo problema subyacente.
En la prueba con ratones, los resultados fueron claros. Administrado por vía oral durante 60 días, NU-9 redujo la inflamación cerebral en múltiples regiones cerebrales, lo que sugiere un amplio efecto antiinflamatorio. Los oligómeros tóxicos unidos a los astrocitos se redujeron drásticamente. La forma anormal de TDP-43 disminuyó. «Estos resultados son asombrosos», afirmó. William Klein, experto en Alzheimer en Northwestern.
“NU-9 tuvo un efecto notable sobre la gliosis astrocítica reactiva, que es la esencia de la neuroinflamación en las primeras etapas de la enfermedad de Alzheimer”.

Una pastilla al día durante dos meses. Funcionó en ratones. Los ensayos en humanos aún están pendientes.
Alzheimer temprano: prevención, no cura. El cambio de paradigma.
Kranz y Silverman comparan el NU-9 con las intervenciones tempranas para el cáncer y las enfermedades cardíacas. No se espera a que el cáncer esté avanzado ni a que se produzca un infarto. Se monitorizan los marcadores, se identifican los riesgos y se interviene antes. Lo mismo podría aplicarse al Alzheimer en sus inicios. Ya se están desarrollando pruebas de diagnóstico de sangre que detectan marcadores proteicos años antes de que aparezcan los síntomas. Combinar estas pruebas con un fármaco preventivo como el NU-9 podría erradicar la enfermedad de raíz.
Obviamente, aún faltan ensayos en humanos. El equipo de Northwestern está probando NU-9 en otros modelos animales, incluyendo ratones que representan mejor el envejecimiento humano típico. Quieren comprender si el tratamiento temprano con NU-9 realmente previene el desarrollo de síntomas a largo plazo. Y quieren verificar los efectos sobre la memoria y la salud neuronal a largo plazo.
Pero la idea subyacente sigue clara: no esperes a que el Alzheimer temprano se convierta en Alzheimer avanzado. Tómalo pronto, mientras el cerebro aún está intacto. Cuando una pastilla diaria puede marcar la diferencia entre recordar y olvidar.
Hace dieciséis años, Silverman buscaba una molécula capaz de prevenir la acumulación de proteínas tóxicas. Ahora la tiene. Se ha probado en ratones, ha funcionado en la ELA y la FDA la ha aprobado para ensayos clínicos. Ahora es el turno del Alzheimer de inicio temprano. Si funciona como se espera, NU-9 podría convertirse en el primer fármaco preventivo contra una enfermedad que aún no tiene cura.
Esa es la diferencia: ya no esperas a enfermarte. Primero tomas la pastilla.
Los oligómeros tóxicos de beta-amiloide son pequeños agregados solubles de la proteína beta-amiloide, compuestos por unos pocos monómeros que se fusionan en el cerebro. A diferencia de las placas más grandes, estos oligómeros son las formas iniciales más dañinas, atacando las sinapsis entre neuronas, interrumpiendo la comunicación celular y causando neurodegeneración en la enfermedad de Alzheimer. ↩︎
_____________________
Gianluca Riccio, directora creativa de Melancia adv, redactora y periodista. Forma parte del Instituto Italiano para el Futuro, World Future Society y H+. Desde 2006 dirige Futuroprossimo.it, el recurso italiano de Futurología. Es socio de Forwardto - Estudios y habilidades para escenarios futuros.
_________
Fuente:




