Los científicos han descubierto que las propias alarmas inmunitarias del cuerpo pueden desempeñar un papel importante en las enfermedades que provocan un envejecimiento prematuro
Crédito: Shutterstock
Scitechdaily.com/
Universidad Hebrea de Jerusalén, 12 de mayo de 2026
Investigadores han identificado una respuesta inmunitaria hiperactiva como un factor importante en la degeneración tisular en trastornos graves de reparación del ADN. Sus hallazgos sugieren que atenuar esta respuesta podría restaurar la función biológica de maneras que desafían las ideas preconcebidas sobre el envejecimiento y el daño celular.
Nuevas investigaciones sugieren que reducir la actividad de un sensor inmunitario hiperactivo puede ayudar a restaurar la función tisular en trastornos genéticos graves, ofreciendo una nueva perspectiva sobre el envejecimiento y el daño al ADN .
El sistema inmunitario está diseñado para reconocer y eliminar virus, pero este mecanismo de defensa a veces puede volverse contra el propio cuerpo. Cuando fragmentos dañados del ADN del organismo se confunden con material viral, el sistema inmunitario puede desencadenar una fuerte respuesta inflamatoria que daña los tejidos sanos.
Un equipo de investigación internacional liderado por la Dra. Marva Bergman y el Prof. Itamar Harel de la Universidad Hebrea, junto con el Prof. Yehuda Tzfati, el Prof. Ido Ben-Ami (Universidad Hebrea y Centro Médico Sha'are Zedek) y la Prof. Bérénice Benayoun (Universidad del Sur de California), identificó esta reacción inmunitaria errónea como una causa importante de la degeneración tisular en trastornos graves de envejecimiento acelerado. Al reducir la falsa alarma inmunitaria, los investigadores restauraron la función en varios sistemas biológicos.
Repensando la causa del declive celular
El estudio se centró en trastornos raros de reparación del daño del ADN (DDR, por sus siglas en inglés), como la ataxia-telangiectasia (AT) y el síndrome de Bloom. Estas afecciones alteran la capacidad del organismo para reparar el daño rutinario del ADN, lo que provoca inestabilidad genómica, neurodegeneración, mayor riesgo de cáncer y envejecimiento prematuro.
Durante muchos años, los científicos creyeron que el daño no reparado en el ADN era el principal responsable del deterioro celular. Los nuevos hallazgos sugieren que la reacción del organismo ante ese daño podría desempeñar un papel igualmente importante.
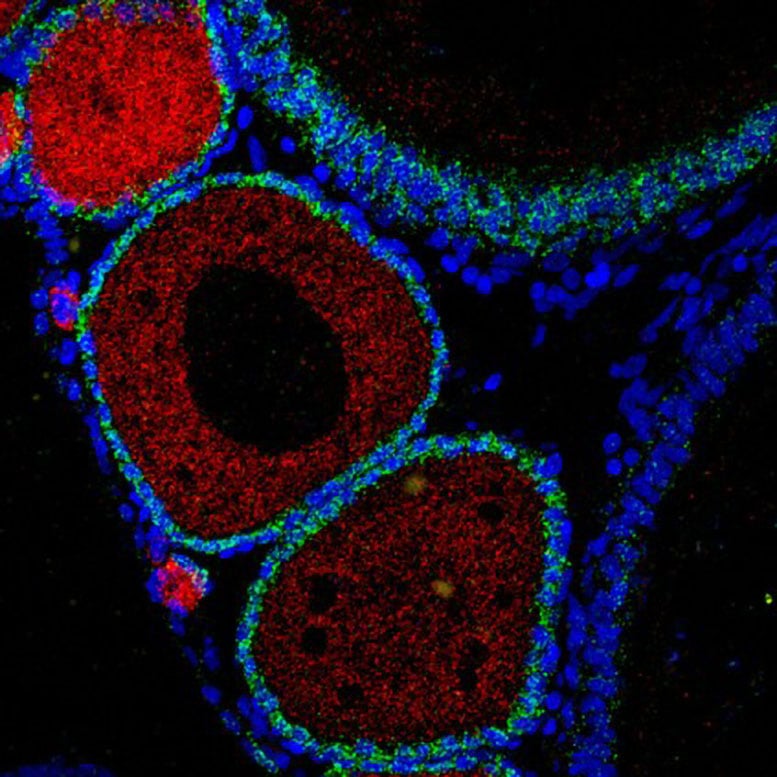 Reversión de los signos del envejecimiento acelerado mediante la supresión de un sistema de alarma celular: hibridación fluorescente in situ de molécula única (smFISH) en ovarios de hembras de pez killi, visualizando los ovocitos inmaduros (ddx4) en rojo y las células de la granulosa (lhr) en verde. Los núcleos son visibles en azul. Crédito: Eitan Moses
Reversión de los signos del envejecimiento acelerado mediante la supresión de un sistema de alarma celular: hibridación fluorescente in situ de molécula única (smFISH) en ovarios de hembras de pez killi, visualizando los ovocitos inmaduros (ddx4) en rojo y las células de la granulosa (lhr) en verde. Los núcleos son visibles en azul. Crédito: Eitan Moses“Nuestros resultados demuestran que el daño no actúa solo”, afirmó el profesor Harel. “Es la respuesta del cuerpo a ese daño, una reacción inflamatoria crónica y exagerada, la que impulsa gran parte de la degeneración”.
Cuando las células no reparan correctamente el ADN, fragmentos de este pueden escapar al citosol, el fluido que rodea las estructuras celulares. Allí, activan un sensor llamado cGAS. Este sistema normalmente detecta el ADN viral, pero no puede distinguir con fiabilidad entre el ADN extraño y el ADN dañado del propio organismo. Como consecuencia, el sistema inmunitario desencadena una respuesta inflamatoria prolongada que, con el tiempo, puede dañar los tejidos.
El doble papel de cGAS
Los investigadores también descubrieron que la cGAS tiene otra función además de desencadenar la inflamación. Esta molécula puede entrar en el núcleo celular e interferir directamente con la reparación del ADN. En condiciones normales, la cGAS ayuda a proteger el organismo, pero cuando se sobreestimula, puede contribuir a un mayor daño.
Para explorar si controlar esta respuesta podría ralentizar la progresión de la enfermedad, el equipo utilizó un modelo de vertebrado de envejecimiento acelerado, comúnmente empleado para estudiar los cambios relacionados con la edad. La disminución de la actividad de cGAS mejoró significativamente varios marcadores de la enfermedad, incluyendo la neuroinflamación, la degeneración tisular y la reducción de la capacidad reproductiva.
Dra. Marva Bergman (izquierda) y Prof. Itamar Harel Crédito: Alon Harel-Katz
«No solo estábamos ralentizando el deterioro», dijo el Dr. Bergman. «Observamos una amplia recuperación de la función tisular. Esto sugiere que el cuerpo puede hacer frente a un mayor daño en el ADN del que suponíamos, si se mantiene bajo control la respuesta inflamatoria».
Implicaciones para el envejecimiento y el tratamiento de enfermedades
Los hallazgos podrían influir en futuras estrategias de tratamiento. En lugar de intentar reparar cada lesión del ADN, los investigadores podrían centrarse en la respuesta inflamatoria del organismo al daño del ADN. Sin embargo, el equipo señaló que la proteína cGAS también es importante para combatir las infecciones virales, por lo que cualquier terapia futura debería reducir la inflamación perjudicial sin debilitar las defensas inmunitarias.
La investigación también podría tener implicaciones más allá de los trastornos genéticos raros. La inflamación crónica y la inestabilidad genómica son características comunes de muchas enfermedades relacionadas con la edad, lo que sugiere que los mismos mecanismos podrían desempeñar un papel más amplio en el envejecimiento.
Estudios relacionados del grupo también analizaron cómo procesos biológicos como la reproducción y el desarrollo cronológico se relacionan con el envejecimiento y la esperanza de vida. En conjunto, los hallazgos respaldan la idea de que los sistemas que benefician al organismo en las primeras etapas de la vida también pueden contribuir al deterioro a largo plazo.
Los investigadores recalcaron que revertir los síntomas de una enfermedad no equivale a ralentizar el proceso natural de envejecimiento. Aun así, el estudio pone de relieve un nuevo enfoque prometedor para el tratamiento de trastornos degenerativos graves mediante la modulación de las vías de señalización inmunitaria del propio organismo.
____________
Referencia:
“Un doble papel del cGAS en la configuración de las respuestas celulares y orgánicas a la inestabilidad genómica” por Marva Bergman, Uri Goshtchevsky, Tehila Atlan, Gwendoline Astre, Ryan Halabi, Hosniyah El Ayoubi, Eitan Moses, Aaron JJ Lemus, Bérénice A. Benayoun, Yehuda Tzfati, Ido Ben-Ami e Itamar Harel, 14 de abril 2026, Genes y Desarrollo .
______
Fuente:





